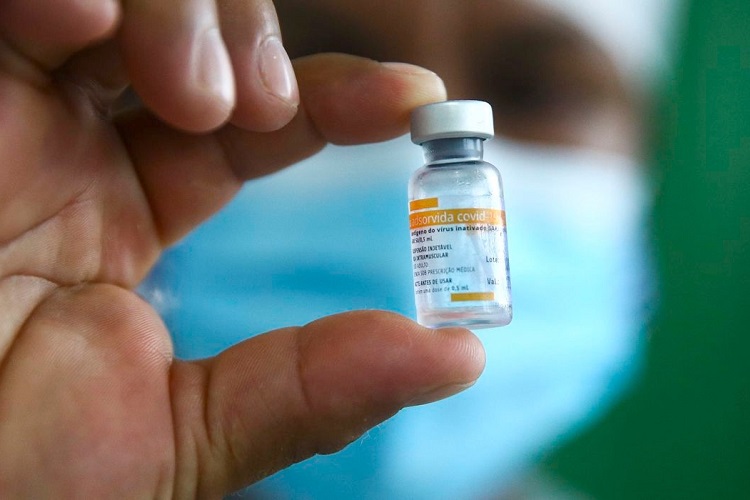
O Ministério da Saúde confirmou nessa sexta-feira, 29, que vai comprar mais 54 milhões de doses da Coronavac, vacina desenvolvida pela farmacêutica chinesa Sinovac e produzida no Brasil pelo Instituto Butantan. O novo lote se somará às 46 milhões de unidades que já foram adquiridas pela União.
Em nota na noite dessa sexta, a pasta disse que vai firmar o contrato de compra das doses junto ao Butantan “semana que vem” e ressaltou que “está solicitando a antecipação do registro da vacina na Anvisa (Agência Nacional de Vigilância Sanitária), para ampliar a vacinação para toda a população”. Por enquanto, a Coronavac tem só autorização de uso emergencial.
LEIA MAIS: MP analisa quase 300 denúncias de casos de fura-fila no Rio Grande do Sul
Publicidade
O Butantan e o governo paulista vinham pressionando o ministério desde o início da semana pela confirmação do novo contrato. O diretor do instituto, Dimas Covas, afirmou que, se a pasta não efetivasse a compra, iria exportar as doses excedentes a países da América Latina.
O governador João Doria (PSDB) disse que, caso o governo federal não manifestasse interesse até semana que vem, as doses poderiam ser vendidas para estados e municípios. O ministério justificava que, por contrato, tinha até maio para decidir sobre o novo lote. A pressão de governadores e prefeitos e as críticas de especialistas sobre a demora na definição pesaram para que a pasta antecipasse a decisão.
LEIA TAMBÉM
Municípios vão receber nova remessa de vacinas na segunda-feira
Em Santa Cruz, sentimento é de esperança entre os imunizados
Publicidade
Registro definitivo da vacina de Oxford foi pedido
A Agência Nacional de Vigilância Sanitária (Anvisa) comunicou também nessa sexta-feira que recebeu o pedido de registro definitivo da vacina produzida pela Universidade de Oxford e pela farmacêutica britânica AstraZeneca, em parceria com a Fundação Oswaldo Cruz (Fiocruz).
O pedido de registro definitivo é diferente da autorização de uso emergencial, que já foi obtida pelo consórcio. Enquanto na última a imunização pode ser feita apenas em grupos específicos, na definitiva o grupo responsável pelo imunizante pode vacinar qualquer indivíduo e comercializar o produto.
Enquanto a autorização emergencial teve sua análise feita em cerca de dez dias, o registro definitivo tem um processo de avaliação mais longo, de até 60 dias. “Devido ao estágio das avaliações já realizadas, buscando superar os prazos legais estabelecidos, a Anvisa manterá total prioridade na análise para fins de concluir o processo no menor tempo possível”, diz a nota da agência.
Publicidade
LEIA TAMBÉM
Mais de duas mil doses da vacina já foram aplicadas em Santa Cruz
Doses são suficientes para vacinar 60% dos profissionais de saúde
Insumos para a CoronaVac devem chegar até o dia 3 de fevereiro
Oxford/AstraZeneca e Fiocruz se mobilizam
Como a Anvisa adotou uma dinâmica contínua, o consórcio Oxford/ AstraZeneca e a Fiocruz já vêm apresentando documentações sobre a vacina. O primeiro pacote de informações foi entregue à agência reguladora em outubro do ano passado.
LEIA TAMBÉM: Fiocruz: ‘sem SUS e conhecimento científico vacinação não seria possível’
Depois de entregar 2 milhões de doses da vacina Oxford/AstraZeneca importadas da Índia, a Fiocruz aguarda a chegada de lotes do Ingrediente Farmacêutico Ativo (IFA) para produzir novos lotes. A perspectiva da fundação é que sejam fabricadas até 50 milhões de doses até abril e 100,4 milhões até julho deste ano.
Publicidade
LEIA MAIS: ACOMPANHE A COBERTURA COMPLETA SOBRE O CORONAVÍRUS